純物質と混合物
前の章でも述べたように、純粋な物質の沸点や融点を測定してみると常に一定の値をしめすものです。
これに対して、2種以上の物質を混ぜた混合物は一定の沸点も融点もしめしません。
そこで、一定の沸点と融点を持つ物質を純粋な物質(純物質)といい一定の沸点や融点を持たない物質を混合物ということに決めます。
混合物の沸点
水やアルコールは、その体積の大小に関わらず同じ温度で沸騰することはすでに学びました。
それでは、水とエチルアルコールを混ぜ合わせたものの沸騰する温度すなわち沸点はあるのでしょうか。
水1に対してエチルアルコール1体積の割合に混合したものをフラスコに入れ1~3個の沸騰石を入れ、温度計を入れて熱してみましょう。
そして、時間と温度との関係をグラフに書いてみます。
水やアルコールを別々に熱したときのグラフに比べ一定の沸点をしめさないことがはっきりわかります。
水に溶けているアルコールが全部蒸発してしまうとはじめて100℃の沸点をしめすようになります。
次に、水に食塩を混合した場合の沸点について、調べてみましょう。
20グラムの水に、2グラムぐらいの食塩を溶かした液を大形の試験管に入れ沸騰石を加え、温度計を入れて熱してみましょう。
そして、やはり温度と時間の関係をグラフに書いてみます。
食塩水は、100℃ぐらいから沸騰をはじめますがその温度はだんだん高くなって、106℃ぐらいになるまで上昇を続けます。
食塩水の底のほうに食塩の結晶がでるまで温度は上昇を続け結晶が出ると、はじめて一定の温度になります。
この2つの例からもわかるように2つの物質を混合した場合は一定の沸点をしめさないものです。
これに対し純粋な物質は、一定の沸点をもっています。
混合物の融点
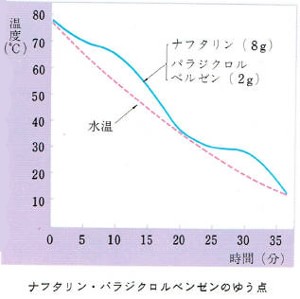
ナフタリソやパラジクロルベンゼンは、一定の融点をもっています。
今、ナフタリンとパラジクロルベンゼンの2物質を混合してその混合物の融点を調べてみましょう。
ナフタリンとパラジクロルベンゼン2グラムの割合で混合し前回と同じ方法で融点を測定します。
グラフを見てわかるように、この混合物は一定の融点を示せません。
純粋な水は、0℃で氷になります。すなわち、氷の融点は0℃です。
水に食塩を溶かした場合や水に砂糖を溶かした場合の融点はどうなるでしょうか。
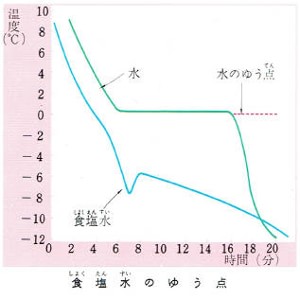
水の融点を測定したのと同じ方法で、食塩水の融点を測定してみましょう。
水20立方センチに食塩5グラムを溶かし、これを大形試験管に入れて温度計を入れ、寒剤の中に入れて冷やします。
温度と時間との関係をグラフにします。
このグラフから、食塩水は一定の融点をしめさないことがわかります。
.
水に他の物質が溶解したときは、0℃より低い温度で氷ができます。
混合する物質が多くなるにつれて、氷のできる温度はいっそう低くなります。
海の水がなかなか凍らないのや漬物の汁が冬に水が凍るような寒いところでも凍らないのはこのためなのです。
また、純粋な酢酸は16.6℃の融点をもっています。
これに、水を加えると、16.6℃になっても凝固しません。
この水を含んだ酢酸が凍る温度は、加えた水の量によってまちまちです。
これも、混合物が一定の融点をしめさない例の一つです。
このように、純粋な物質はそれが純粋でありさえずれば、どの試料を測定してもいつも一定の融点をしめすのに対し混合物はその混合の割合により融点が異なりグラフに書いた場合も、純粋な物質とは違う温度の下がり方をしたり融点がはっきりしなかったりします。