硝酸の工業的製法
硝酸は、アンモニアを空気とまぜ約800℃に熱した白金触媒の上で燃やしたものを水に溶かしてつくります。
このときの化学変化は、非常に複雑ですがまとめると図の式のようになります。
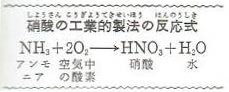
この方法でつくった硝酸は、純粋で濃いすぐれたものです。
現在では、ほとんどの硝酸がこの方法で製造されていますがむかしは、硝酸カリウムや硝酸ナトリウムに硫酸をくわえそれを蒸留してつくっていました。
しかし、この方法はアンモニアから製造するのにくらべて原料や費用の点ではるかに劣るので現在では行われていません。
硝酸の実験室的製法
実験室では、ふつう硝酸カリウムや硝酸ナトリウムに硫酸を注ぐ方法で硝酸をつくっています。
レトルトに、粉にした硝酸カリウムを30グラムほど入れこれに濃硫酸20立方センチをくわえます。
レトルトは石綿金網か砂ざらの上におきその先を冷たい水で冷やした受器にさしこんでおきます。
そして。レトルトを静かに熱すると硝酸の蒸気が受器に入りそこで冷やされて液状になります。
受器には、いつも冷水がかかるようにしておかなければなりません。
このときの反応は温度が比較的低いと①式のようにすすみます。
また、温度が高いと、②式のように反応します。
硝酸ナトリウムから硝酸をつくるときの反応も硝酸カリウムからつくる場合と同じです。
硝酸の性質
純粋な硝酸は、硝酸の蒸気による刺激臭のある無色の液体で、比重は1.52です。
硝酸は、湿気を吸う性質が非常に強く空気中では煙をだします。
日本薬局方の濃硝酸は、約25パーセントのものですがこれを2倍の容積の水でうすめると、使いやすくなります。
また実験室では、ふつう濃硝酸を12倍の水でうすめた希硝酸を使っています。
濃硝酸には、いろいろな有機化合物に作用する性質があります。
この作用を硝化作用、またはニトロ化作用といいます。
繊維素(セルロース)に作用させると火薬やセルロイドの原料になるニトロセルロースができグリセリンに作用させると、火薬原料のニトログリセリンができます。
このほか、たんぱく質に作用して、黄色にする性質がありこれをキサソトプロテイン反応といいます。
硝酸がつくと、皮膚や爪などが黄色くなるのはこの反応のためです。
硝酸の用途
硝酸は、火薬・染料・セルロイドなどの製造に使われるほかアンモニアと作用させて、硝酸アンモニウム(硝安)をつくります。
硝酸アンモニウムは、非常に窒素分の多い肥料で硫酸アンモニウムにかわる窒素肥料として重要になってきています。
また、硝酸を、塩基や金属酸化物に作用させると硝酸塩ができます。
硝酸塩は大切な化学薬品で、水によく溶ける性質をもっています。


