 塩のでき方
塩のでき方 塩のいろいろなでき方とは? わかりやすく解説!
塩酸に水酸化ナトリウムの水溶液をくわえて中和させると塩として、塩化ナトリウム(食塩)ができることがわかりました。
この塩のでき方について、もう少しくわしく調べてみます。
(adsbygoogle = window.ads...
 塩のでき方
塩のでき方  塩のでき方
塩のでき方  酸・塩基
酸・塩基  酸・塩基
酸・塩基  酸・塩基
酸・塩基  金属の酸化と還元
金属の酸化と還元  水と物の溶け方
水と物の溶け方  水と物の溶け方
水と物の溶け方  水と物の溶け方
水と物の溶け方  水と物の溶け方
水と物の溶け方  水と物の溶け方
水と物の溶け方  水と物の溶け方
水と物の溶け方 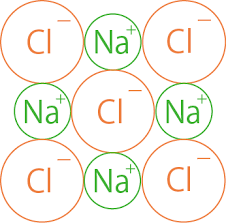 水と物の溶け方
水と物の溶け方  水と物の成立ち
水と物の成立ち