溶液の沸点と氷点
純粋な水に、一気圧のもとでは、0℃以下では氷になりますが100℃になると沸騰して水蒸気にかわります。
このことを、水の氷点(融点)は0℃であり、沸点は100℃であるといいます。
しかし、水にいろいろな物質が溶解しているとこの溶液の氷点や沸点は、純粋な水のときと違ってきます。
ビーカーに純粋な水を入れ、沸騰しているときの温度をはかりつぎに、砂糖を溶かして沸騰させ、その温度をはかって水のときと比べると違いがよくわかります。
溶質が砂糖や塩化ナトリウムのように固体であるときは、その水溶液の氷点は0℃以下となり沸点は100℃を越えるようになります。
つぎのグラフは、砂糖の水溶液の氷点と沸点とをしめしたものです。
このグラフから、氷点の下がる程度や沸点の上がる程度は、溶かした砂糖の重さに比例していることがわかるでしょう。
このことを利用して、分子量がわからない物質の分子量を実験によってもとめることもできるのです。
ここでは、純粋な溶媒に他の物質を溶かしたときに沸点や氷点(融点)がかわるということを覚えておいて下さい。
溶液の濃度
物質の溶け方を注意してみると砂糖のように非常に水に溶けやすいものと塩化ナトリウム(食塩)のようにそれほどよく溶けないものとがあります。
そこで、ある溶媒に溶質がどれだけ溶けるかとかこの溶液には溶質がどれだけ、溶けているかとかをあらわすのに溶液の濃さをはかる基準を決めておくと、たいへん便利です。
この基準を濃度といいます。
濃度のあらわし方としては、ふつうパーセント濃度が使われます。
パーセント濃度は、つぎの式のようにして計算します。
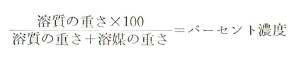
ここで注意しなければならないのはパーセント濃度は、溶質の溶液にたいする割合であって溶質の溶媒にたいする割合ではないということです。
また、濃度をあらわすのに溶液1リットルに溶けている溶質のグラム数を溶質の分子量で割った値を使うこともあります。
コロイド溶液
溶液中の溶質は分子の大きさで溶媒中に散らばっています。
そして、この溶液は色のついていることはありますがすべて透明です。
また、ろ紙を自由に通り抜けます。
ところが、溶液中に散らばっている粒子が1ミリの100万分の1から1万分の1ぐらいの大きさになるとろ紙は通り抜けますが、光の進む道をさえぎるようになります。
このくらいの大きさの粒子には1粒に原子が1000から10億個ぐらいふくまれていてコロイド粒子といわれます。
また、このコロイド粒子を含んでいる溶液をコロイド溶液といって、ふつうの溶液とは区別しています。
コロイド粒子は、ろ紙は通り抜けますがろ紙より目の細かいセロハンやポリニチレンの膜などは通り抜けません。
コロイド溶液に、細い光の筋を当てると光の進む道が、ぼんやりとにごって見えます。
このように、コロイド溶液に光の筋を当てて光の進む道が見える現象をチンダル現象といいます。
また、コロイド粒子はふつうの顕微鏡では見ることができませんが限外顕微鏡という特別な装置をつけた顕微鏡で見ると粒子のひとつひとつが光の点となって見えます。
この粒子をよく見るとひとつひとつが、あちこちと不規則に動き周っているのがわかります。
この粒子の運動を、ブラウン運動といいます。
チンダル現象とブラウン運動はコロイド粒子にだけ見られる特別な性質です。


