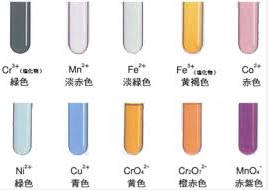
水溶液中に、あるイオンが溶けているときそれが何のイオンであるかを調べることを、イオンの検出といいます。
ここでは金属イオンの検出について、調べてみましょう。
イオンには、他のイオンと反応して、気体になるとか沈殿を生ずるとか色をしめすというような特有の反応があります。
イオンの検出は、このイオン特有の反応を利用しておこないます。
ふつう、検出しようとするイオンのほかにほかのイオンがまざっている場合が多いのでそれらが検出の邪魔になるときは、あらかじめ分離しておきます。
つぎに、検出しようとするイオンに特有な反応をおこなわせてそのイオンの存在を確認します。
確認のためには、沈殿をつくり、その色や性質を調べたり特有な色をしめす複雑なつくりのイオンをつくったりします。
そのイオン特有の鋭敏な反応を選べば試験管やビーカーを使わずに石紙や時計ざらの上ででも確実に、わずかな量のイオンを調べることができます。
そのほか炎色反応なども、操作がかんたんなので検出の補助手段として使われます。
金属イオンの反応
おもな金属イオンについて、それぞれの特有な反応を調べてみましょう。
実験するときは、それぞれのイオンをふくむ溶液(硝酸塩などの2パーセソト溶液)を用いておこないます。
銀イオン
Ag+ 無色のイオン。
① 塩酸や塩化ナトリウムの水溶液などのような塩素イオンをふくむ溶液をくわえると、白色の塩化銀が沈殿します。
塩化銀は光にあたると一部が分解し、細かい銀の粒ができるため紫色に変色します。
塩化銀は、アンモニア水に溶けます。
この溶けた溶液に、ヨウ化カリウム溶液をくわえると、黄色のヨウ化銀が沈殿します。
アンモニア水をくわえすぎていた場合は、白色の沈殿に見えます。
② うすいアンモニア水をくわえると褐色の酸化が沈殿しさらにアンモニア水をくわえると無色の銀アンモニア錯イオンをつくって溶けてしまいます。
酸化銀ができた溶液をそのままにしておくと、爆発性物質ができるので、注意が必要です。
③ うすい水酸化ナトリウム溶液をくわえると、酸化銀が沈殿しさらにくわえても、沈殿は溶けません。
④ ヨウ化カリウム溶液をくわえるとヨウ化銀ンの黄色沈殿ができます。
ヨウ化銀は、硝酸やアンモニア水には溶けません。
銅イオン
Cu2+ 水溶液は青色をしめします。
① うすいアンモニア水をくわえると、うすい青色の水酸化第二銅のが沈殿します。
しかし、アンモニア水をさらにくわえると濃い青色の銅アンモニア錯イオンをつくって溶けます。
② うすい水酸化ナトリウム溶液をくわえると水酸化第二銅が沈殿しますがさらにくわえても溶けません。
③ 炎色反応は、緑色をしめします。
アルミニウムイオン
Al3+ 無色。
① うすいアンモニア水をくわえると白色の寒天のような水酸化アルミニウムが沈殿します。
② うすい水酸化ナトリウム溶液をくわえると水酸化アルミニウムの沈殿ができますが、さらにくわえると、アルミン酸イオンができて溶けます。
この溶液を酸で中和すると、また水酸化アルミニウムが沈殿しますが酸を多くくわえると溶けます。
第二鉄イオン
Fe3+ 水溶液は、黄色をしめします。
① うすいアンモニア水や、水酸化ナトリウム溶液をくわえると赤褐色の水酸化第二鉄が沈殿し、さらにくわえても溶けません。
② フェロシアン化カリウム溶液をくわえると、濃い青色の沈殿をつくります。
バリウムイオン
Ba2+ 無色のイオン。
① うすい硫酸をくわえると、白色の硫酸バリウムが沈殿しこれは酸にも、塩基にも溶けません。
② 炭酸アンモニウム溶液をくわえると、炭酸イオンと反応して白色の炭酸バリウムが沈殿します。
これに、うすい酸をくわえると二酸化炭素を発生しながら溶けてしまいます。
③ 炎色反応は、うすい緑色をしめしまします。