濃い酸のはたらき
うすい酸のはたらきを調べたときと同じようにして濃硫酸や濃塩酸のはたらきを調べてみましょう。
濃硫酸と濃塩酸は、どちらも取扱いには、充分注意しましょう。
亜鉛・鉄・スズ・銅を濃い酸に入れた場合いの結果をまとめるとつぎのようになります。
① 亜鉛・鉄・スズは、水素を発生して濃塩酸に溶けます。
スズは、濃硫酸にほとんど溶けません。
② 銅は、濃塩酸には溶けませんが、濃硫酸にはゆっくり溶けます。
亜鉛・鉄も溶けます。
このとき発生する気体には、刺激臭があります。
それは、この気体に二酸化硫黄がふくまれているからです。
濃硫酸との反応は、温度が低いとはっきりしませんが加熱するとよくわかります。
いっぽう、銅は、濃塩酸には溶けませんが濃硫酸には、二酸化硫黄を発生して溶けます。
濃塩酸の場合の反応は、希塩酸のときとまったく同じですが、濃硫酸の場合に、反応のしかたが少し違います。
まえに述べたように、硫酸は強い酸化力をもっています。
その性質は希硫酸ではあまりあらわれませんが濃硫酸では強くあらわれてきます。
たとえば、銅を濃硫酸に入れると銅の表面はすぐに酸化されて、図の①式のように酸化第二銅になります。

このとき、硫酸自身も変化して、二酸化硫黄を発生します。
こうしてできた酸化第二銅は、すぐに酸が電離してできている水素イオンと作用して、②式のように第二銅イオンとなって水に溶けます。
硝酸も.硫酸と同じように、非常に酸化力が強いのでもともと酸に溶けない銅や銀などの金属を酸化銅や酸化銀などの酸化物にかえて溶かしてしまう性質をもっています。
王水
銅や銀は、濃硝酸を使って酸化物にして溶かすことができますが金や白金は、硝酸の酸化力では酸化することができません。
ところが、濃硝酸と濃塩酸を1対3の割合でまぜた液を使うと金や白金も溶かすことができます。
この混合液を王水といいます。
王水の中には、硝酸と塩酸が化合して塩化ニトロシルという、非常に酸化力の強い化合物ができこれが、金や白金を塩化物にかえるはたらきをしてこの塩化物が塩酸に溶けるのです。
金属酸化物への酸のはたらき
濃い酸のはたらきで調べたように、イオン化傾向が小さくてそのままでは酸に溶けない金属でも、酸化剤で酸化物にかえると溶けるようになります。
つまり、金属の酸化物は、金属そのものよりも水素イオンと反応しやすいわけです。
この金属の酸化物と酸の反応について、もう少しくわしく調べてみましょう。
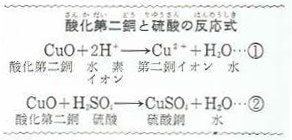
酸化第二銅に硫酸が作用する場合を考えてみます。
酸化第二銅は.硫酸が電離してできた水素イオンと反応して、上の①式のように、第二銅イオンになります。
硫酸は完全に電離して、水素イオンと硫酸水素イオンになりさらに硫酸水素イオンの一部は水素イオンと硫酸イオンとに電離しています。
酸化第二銅と硫酸との反応をまとめると②式のようにあらわすことができます。
この溶液をに詰めると、銅イオンと硫酸イオンとがむすびついて、硫酸銅の結晶ができます。
酸化第二銅は、塩基ではありませんが、この変化は酸と塩基の中和反応によくにています。
それで、中和反応でできる物質を塩というように硫酸銅を銅の硫酸塩といいます。
このように、金属の酸化物を酸に溶かすと金属とその酸の塩ができます。


