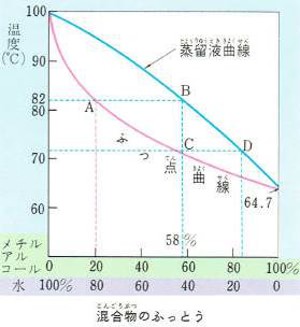
液体にして分離する方法
空気は、窒素・酸素、その他の気体の混合物ですが、これに圧力をかけて、冷やすと、液体空気が得られます。
液体空気の中にある液体窒素も液体酸素もそれぞれ違った沸点をもっていますからこれを放置しておくと、沸点の低いヘリウムやネオンが気体となって蒸発し続いて窒素・アルゴンが蒸発します。
残った液には、酸素が多く含まれますがこれが蒸発すると、クリプトンやキセノンなどの液体が残ります。
このような方法でそれぞれの気体を分離することができます。
また、アンモニアと水素や窒素の混合気体を冷やすとアンモニアは液体になり、他は気体のままでいるのでアンモニアを分離することができます。
このように気体混合物は、その全部を液体にしてから分留するか液化しやすい気体だけを液化して分離します。
吸収剤・吸着剤などで分離する方法
二酸化炭素と酸素の混合気体から酸素だけを分離するにはつぎのようにします。
混合気体を注射器に入れ、二酸化炭素をよく吸収する液(水酸化ナトリウムや水酸化カリウムの濃い水溶液)を吸い込み栓をしてよく振ります。
すると、二酸化炭素は、それらの液に溶けるので気体の体積は小さくなり、酸素だけが残ります。
空気中の酸素の量を測定する
窒素の混合気体から、酸素を取り除くには、つぎのようにします。
酸素は、塩基性にしたピロガロールの水溶液(ピロガロールの5%水溶液と10%水酸化ナトリウム水溶液を1対1に混ぜたもの)に吸収されるのでまえのように注射器に入れて振ると、酸素は吸収され窒素だけが分離します。
この方法を用いると、空気中の酸素の量を測定することができます。
すなわち、注射器にとってはじめの空気の体積V1をはかっておき、つぎにピロガロールを入れて、これに吸収された酸素の体積2をはかればV2/V1 が空気中の酸素の割合となります。
また、つぎのような方法もあります。
繊維状の鉄(スチールウール)を試験管に入れ水の中に逆さまに立てておくと、空気中の酸素はスチールウールをさびさせるのに使われてしまいます。
そのため、使われた酸素の量(体積)だけ水が試験管の中に入りますからその体積から酸素の量を測定することができます。